L'alumine est l'une des céramiques les plus populaires du marché. Selon une étude de marché, la taille du marché mondial de l'alumine a atteint 44,73 milliards de yuans en 2024, et devrait atteindre 46,83 milliards de dollars américains en 2025, et devrait dépasser 70,8 milliards de dollars américains en 2034. Cela montre l'importance de l'alumine en tant que matériau.
Dans ce guide, vous apprendrez tout sur l'alumine. Des procédés de fabrication aux propriétés, en passant par les types et les applications, vous trouverez ici de nombreuses informations à son sujet.
Liens rapides
- Qu'est-ce que l'oxyde d'aluminium ?
- Structure chimique de l'oxyde d'aluminium
- Procédé de production d'alumine
- Propriétés de l'oxyde d'aluminium
- Types d'oxyde d'aluminium
- Utilisations de l'oxyde d'aluminium
Qu'est-ce que l'oxyde d'aluminium ?
L'alumine est un composé précieux extrait de la bauxite. Elle est composée de deux éléments : l'oxygène et l'aluminium. L'alumine naturelle se présente sous forme de solide cristallin. L'alumine transformée se présente sous forme de poudre blanche. Elle est insoluble dans l'eau et d'autres solvants courants tels que le propanol et l'éthanol (cette propriété s'applique à la plupart des oxydes métalliques). De plus, l'alumine est classée comme un composé amphotère car elle peut réagir avec les bases et les acides.
Réaction avec un acide fort : Al2O3 + 6HCl → 2AlCl3 + 3H2O
Réaction avec une base forte : Al2O3 + 2NaOH → 2NaAlO2 + H2O

Poudre d'alumine blanche
Les autres noms de l'oxyde d'aluminium incluent : l'alumine, l'oxyde d'aluminium (III), l'aloxite ainsi que l'aloxyde
Termes industriels : Aloxite, Alundum
Nom minéralogique : Corindon
Structure chimique de l'oxyde d'aluminium
Structure chimique et formule moléculaire
La formule chimique de l'oxyde d'aluminium est Al₂O₃. Substance inorganique importante, l'oxyde d'aluminium présente une structure moléculaire unique. Sa masse moléculaire est de 101,96 g/mol et son rapport stœchiométrique est Al:O = 2:3.
Sa configuration électronique s'exprime comme :
Al³⁺: [Ne]
O²⁻: [Ne]2s²2p⁶
Les composés sont généralement représentés par des formules chimiques, qui aident à montrer les proportions des atomes individuels présents dans les éléments d'un composé particulier.
Prenons l'exemple de l'oxyde d'aluminium. Sa formule chimique est Al₂O₃. Dans ce cas, les indices 2 et 3 indiquent le nombre d'atomes des deux éléments échangés, ce qui explique la présence de liaisons ioniques dans l'oxyde d'aluminium.
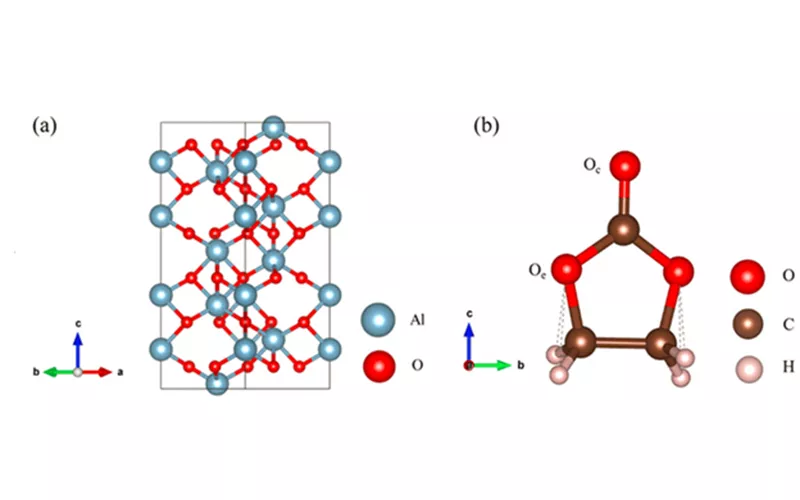
Structure de l'oxyde d'aluminium
Structure cristalline de l'alumine
L'alumine présente de nombreuses formes cristallines, la plus courante étant l'α-Al₂O₃ (corindon), qui est organisé en ions oxygène hexagonaux compacts. Sa structure hexagonale ressemble à un cristal, ce qui explique sa grande dureté.
La structure α-Al2O3 présente les caractéristiques suivantes :
- Réseau hexagonal compact d'ions oxygène ;
- Les ions aluminium occupent 2/3 des vides octaédriques ;
- Paramètres de cellule unitaire : a = 4,758 Å, c = 12,991 Å ;
- Groupe spatial : R3c
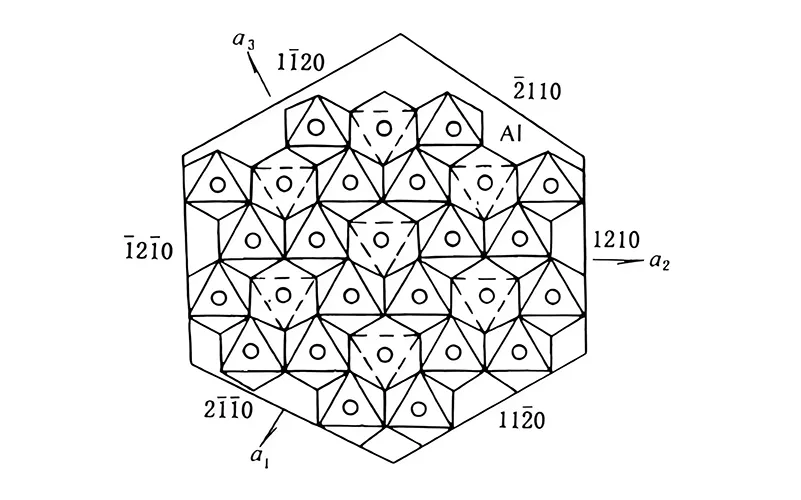
Structure de l'α-Al2O3
En plus de l'α-Al2O3, l'alumine possède également d'autres phases cristallines importantes, comme suit :
- γ-Al2O3 : structure spinelle cubique
- θ-Al2O3 : système monoclinique
- δ-Al2O3 : structure tétragonale ou orthorhombique
- κ-Al2O3 : structure orthorhombique
Chaque phase cristalline possède ses propres propriétés uniques !
Procédé de production d'alumine
Vous êtes curieux de savoir comment fabriquer de l'alumine ? Cette section explique en détail le procédé de fabrication de l'alumine. procédé Bayer C'est l'une des méthodes les plus importantes de production industrielle d'alumine. Elle a été inventée par Karl Josef Bayer en 1887.
L'aluminium métallique réagissant facilement avec l'oxygène de l'air pour former un composé, l'alumine, le procédé Bayer constitue une méthode de purification idéale. Cette méthode utilise la bauxite comme matière première. Son objectif principal est de séparer l'alumine des impuretés telles que le fer, le titane et le dioxyde de silicium. Après une série de traitements chimiques, une alumine de haute pureté peut être obtenue.
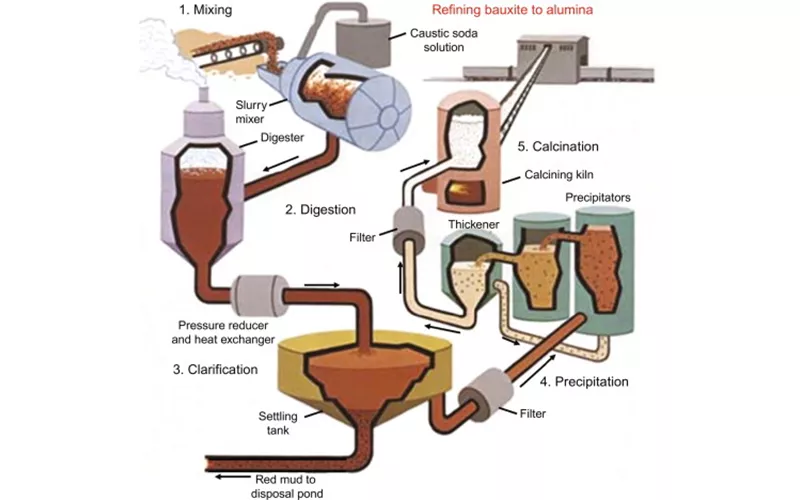
Étape de digestion
Lors de l'étape de digestion, l'alumine est mélangée à une solution concentrée d'hydroxyde de sodium. Une fois les composants de la bauxite dissous dans l'hydroxyde de sodium, ils peuvent être séparés par filtration.
Traitement des matières premières : écraser la bauxite à moins de 200 mesh, mélanger avec une solution d'hydroxyde de sodium et traiter à 160-180℃ et 3,5-4,5MPa de pression.
Réaction chimique : Al2O3·xH2O + 2NaOH → 2NaAlO2 + (x+1)H2O
Contrôle des paramètres clés : précision de la température contrôlée à ±2℃ ; concentration de la solution de Na2O 300-350 g/L ; temps de réaction 1-2
Étape de filtration :
L'étape de filtration consiste à éliminer les impuretés du filtrat, laissant de l'alumine pure, mais veuillez noter que cette méthode n'est pas la plus efficace et qu'elle n'élimine pas toutes les impuretés.
Séparation solide-liquide : Utiliser des filtres haute pression pour séparer les boues rouges et la solution d'aluminate de sodium
Contrôle du processus : La température de filtration est contrôlée à 95-105℃, la pression est contrôlée à 0,4-0,6MPa et la vitesse de filtration est contrôlée à 8-12m3/(m2·h)
Traitement aux boues rouges : Laver et récupérer la solution alcaline et utiliser pleinement la boue rouge.
Stade de précipitation :
Ce processus nécessite le refroidissement de l'oxyde d'aluminium pour précipiter. Lorsque de petits cristaux d'oxyde d'aluminium se forment, le refroidissement est interrompu. On peut également accélérer ce processus en utilisant de l'hydroxyde d'aluminium comme catalyseur.
Ajout de graines : Ajouter 60-80 µm de graines à un ratio de 30-50 g/L
Conditions de précipitations : Précipité à 45-55℃ pendant 24 à 36 heures, valeur du pH contrôlée entre 13,5 et 14,0
Réaction chimique : 2NaAlO2 + 4H2O → 2Al(OH)3↓ + 2NaOH
Étape de calcination :
Ce procédé nécessite de chauffer l'alumine jusqu'à élimination complète de l'eau de cristallisation. Cette étape permet de transformer l'alumine hydratée en alumine anhydre.
Calcination dans l'air à haute température à 1000-1200℃ pendant 1 à 2 heures
Réaction chimique : 2Al(OH)3 → Al2O3 + 3H2O
Les étapes ci-dessus décrivent les étapes simples de préparation de l'alumine par le procédé Bayer. Outre le procédé Bayer, il existe de nombreux autres procédés, tels que le frittage, la lixiviation, le procédé hydrothermal, etc.
Propriétés de l'oxyde d'aluminium
L'oxyde d'aluminium présente diverses propriétés chimiques et physiques. Voici quelques-unes de ses propriétés les plus courantes.
Vous trouverez ci-joint le tableau des paramètres de performance de l'alumine pour votre simple référence.
|
Propriétés du matériau alumine |
|||||||||
|
Nom |
Alumine (Al2O3) |
Propriétés mécaniques |
Charge de dureté Vickers 500 g |
(moyenne générale) |
13.7 |
||||
|
Couleur |
Blanc |
Résistance à la flexion |
MPa |
350 |
|||||
|
Caractéristiques principales |
Résistance aux hautes températures |
Résistance à la compression |
MPa |
– |
|||||
|
Haute isolation |
Module d'élasticité de Young |
moyenne générale |
320 |
||||||
|
Résistance à la corrosion |
coefficient de Poisson |
– |
0.23 |
||||||
|
Haute résistance mécanique |
Ténacité à la rupture |
MPa·√m |
– |
||||||
|
Densité apparente |
(Kg/m³) |
3,7 × 103 |
Caractéristiques électriques |
Rigidité diélectrique |
V/m |
15 × 10⁶ |
|||
|
Absorption d'eau |
% |
0 |
Résistivité volumique |
20℃ |
Ω·cm |
>10¹⁴ |
|||
|
Propriétés thermiques |
Coefficient de dilatation linéaire |
40-400℃ |
×10⁻⁶/°C |
7.2 |
300℃ |
10¹⁰ |
|||
|
40-800℃ |
7.9 |
500℃ |
10⁸ |
||||||
|
Conductivité thermique |
Poids/m³·K |
24 |
Constante diélectrique (1 MHz) |
– |
9.4 |
||||
|
Chaleur spécifique |
J/Kg·K |
0,78 × 10³ |
Tangente de perte diélectrique (1 MHz, ×10⁻⁴) |
(×10⁻⁴) |
4 |
||||
|
Résistance aux chocs thermiques (dans l'eau) |
°C |
200 |
Coefficient de perte |
(×10⁻⁴) |
38 |
||||
Propriétés mécaniques
L'oxyde d'aluminium présente une excellente dureté, contrairement à d'autres composés métalliques. Cette propriété en fait donc un composé adapté à de nombreuses applications industrielles.
Vous pouvez utiliser de l'oxyde d'aluminium dans ;
- Fabrication d'abrasifs industriels
- Fabrication industrielle d'outils de coupe et de meulage.
- Activated alumina-based desiccants (commonly used in packaging machinery for filling desiccants)
De plus, l'oxyde d'aluminium est également un élément approprié dans les industries de la métallurgie, pour la fabrication de matériaux de finition et de mise en forme.
Dureté et résistance
Dureté Vickers :
- Pureté 99,5% : 15-17 GPa
- Pureté 99,9% : 18-20 GPa
Résistance à la flexion :
- Température ambiante : 300-400 MPa
- 1000°C : 150-200 MPa
Ténacité à la rupture :
- 3,5-4,5 MPa·m½
- Plus la pureté de l'alumine est élevée, meilleure est sa ténacité.
Point d'ébullition
Le point d'ébullition de l'oxyde d'aluminium diffère considérablement de celui des autres oxydes métalliques. En conditions normales, son point d'ébullition est de 2977 °C. Il peut donc être utilisé dans des applications nécessitant des températures élevées.
Il s'agit notamment de la fabrication de pièces de chaudières, utilisées comme abrasifs dans la fabrication de papier de verre, et de la production de fours.
Point d'ébullition : 2977°C ±10°C
Température de transition de phase :
- Transition de phase γ→α : ~1000°C
- Transition de phase θ→α : ~1150°C
Point de fusion
Le point de fusion d'Al₂O₃ est d'environ 2072 °C. Ce point de fusion élevé est dû aux fortes liaisons ioniques présentes au sein des molécules.
L'oxyde d'aluminium peut être utilisé dans diverses applications industrielles nécessitant des points de fusion élevés, notamment la fabrication du verre, les fours et la construction de fourneaux.
- Point de fusion: 2072°C ±5°C
Lectures complémentaires : Points de fusion de plusieurs matériaux céramiques
Densité
L'oxyde d'aluminium présente une densité plus élevée que les autres oxydes métalliques. Sa densité varie généralement entre 3,90 et 4,2 g/cm³. La variation de densité de l'oxyde d'aluminium dépend du type d'impuretés et de la structure du métal.
Structure cristalline
La structure cristalline des atomes de l'oxyde d'aluminium présente une structure hexagonale. De plus, la proportion d'anions oxygène et de cations aluminium dans le composé est de 3:2. Cela signifie que pour trois atomes d'oxygène, on trouve deux atomes d'aluminium.
Stabilité chimique
La stabilité chimique de l'oxyde d'aluminium fait référence à son degré de réaction avec d'autres éléments. Dans ce cas, l'oxyde d'aluminium est un oxyde métallique hautement réactif. En effet, l'aluminium métallique réagit facilement avec l'oxygène de l'air pour former un composé stable (oxyde d'aluminium).
Isolation
Les propriétés isolantes de l'oxyde d'aluminium en font un isolant parfait dans de nombreuses applications industrielles. Par exemple, la plupart des isolations électriques reposent sur l'oxyde d'aluminium. condensateurs, ainsi que d'autres circuits intégrés.
Au contraire, malgré une excellente isolation électrique, l’oxyde d’aluminium est un mauvais conducteur de chaleur.
Résistivité volumique :
- Température ambiante : >10¹⁴ Ω·cm
- 1000°C : ~10⁸ Ω·cm
Résistance à la rupture :
- 10-15 kV/mm (température ambiante)
- Diminuera avec l'augmentation de la température
Types d'oxyde d'aluminium
Il existe différents types d'oxydes d'aluminium. Chacun possède des propriétés uniques. Voici quelques-uns des principaux types d'oxydes d'aluminium :
Corindon
Il s'agit d'un type particulier d'oxyde d'aluminium qui se présente sous forme de cristaux. Le corindon est donc une forme impure d'alumine. Il contient d'autres composants tels que le chrome et le fer, entre autres.
Ces impuretés déterminent le type de couleur de l'oxyde d'aluminium. Par exemple, la couleur rouge de l'alumine confirme la présence de chrome.
De plus, l'oxyde d'aluminium riche en chrome est classé dans la variété rubis. Par ailleurs, l'alumine peut présenter une variété de couleurs, contrairement à la variété rubis. Ces types sont classés dans la catégorie des saphirs.
La dureté et la ténacité sont les propriétés dominantes des corindons. Ces propriétés les rendent adaptés à la plupart des applications abrasives, comme la fabrication de papiers de verre.
Caractéristiques de base :
- Composant principal : α-Al2O3
- Système cristallin : système trigonal
- Couleur : incolore (pur) et couleurs variées (contenant des impuretés telles que le fer, le chrome, etc.)
Caractéristiques de performance :
- Dureté Mohs : 9
- Densité : 3,95-4,1 g/cm³
- Très grande stabilité chimique
- Excellente résistance à l'usure
Principales applications :
- Abrasifs haut de gamme, papier de verre
- Matériaux optiques
- Décoration en pierres précieuses (rubis, saphir)
- Applications de céramique de précision

Boehmite
La boehmite, communément appelée hydroxyde d'aluminium, se présente sous la forme d'un mélange de différentes couleurs allant du brun au jaune, en passant par le blanc et le rouge.
La différenciation des couleurs est attribuée à la composition des impuretés dans le minerai métallique.
La boehmite est relativement moins dure et résistante que le corindon.
Pour cette raison, la boehmite ne convient pas à la fabrication industrielle de matériaux abrasifs.
Caractéristiques de base :
- Composant principal : γ-AlO(OH)
- Structure cristalline : système orthorhombique
- Aspect : blanc ou marron clair
Caractéristiques de performance :
- Bonne stabilité thermique
- Surface spécifique élevée
- Structure des pores contrôlable
- Excellente dispersibilité
Principales applications :
- Support de catalyseur
- Adsorbant
- Revêtement
Matériau ignifuge

Diaspore
L'oxyde d'aluminium diaspore est parfois appelé diasporite. La diasporite se présente sous forme de cristaux blancs de taille généralement uniforme.
Contrairement à la boehmite, les diasporites sont relativement plus dures et présentent une résistance à la traction plus élevée. Cependant, malgré leur résistance à la traction élevée, les diasporites présentent une faible ténacité. Ceci explique leur nature généralement très fragile. De même, elles sont insolubles dans l'eau et dans d'autres solvants universels.
Caractéristiques de base :
- Composant principal : α-AlO(OH)
- Structure cristalline : système orthorhombique
- Couleur : blanc, gris ou marron clair
Caractéristiques de performance :
- Bonne résistance au feu
- Haute résistance mécanique
- Propriétés chimiques stables
- Faible coefficient de dilatation thermique
Principales applications :
- Divers matériaux réfractaires
- Applications céramiques à haute température
- Ciment spécial
- Matériaux de broyage

Gamma-Alumine
Il s'agit d'un type particulier d'oxyde d'aluminium couramment utilisé dans l'industrie pétrolière. Il se présente naturellement sous forme de cristaux blancs, ressemblant ainsi à de l'alumine pure.
Une propriété remarquable de l'alumine gamma est sa capacité à se dissoudre facilement dans les bases et les acides. De plus, ce type d'alumine se dissout facilement dans l'eau pour former une solution.
Caractéristiques de base :
- Formule chimique : γ-Al2O3
- Structure cristalline : type spinelle cubique
- Surface spécifique : 150-300 m²/g
Caractéristiques de performance :
- Surface spécifique élevée
- Forte activité catalytique
- Bonne stabilité thermique
- Structure poreuse
Principales applications :
- Support de catalyseur
- Adsorbant
- déshydratant
- Traitement de surface
Alpha-Alumine
Sa porosité, sa conductivité thermique et sa densité diffèrent de celles de l'alumine gamma. En général, l'alumine alpha est plus dense, présente une bonne conductivité thermique et est solide, contrairement à l'alumine gamma.
Caractéristiques de base :
- Formule chimique : α-Al2O3
- Structure cristalline : Hexagonale compacte
- Pureté : Généralement > 99,5%
Caractéristiques de performance :
- La phase d'alumine la plus stable
- Excellentes propriétés mécaniques
- Stabilité à haute température
- Chimiquement inerte
Principales applications :
- Céramiques hautes performances
- Substrats électroniques
- Biocéramique
- Dispositifs optiques
Utilisations de l'oxyde d'aluminium
L'oxyde d'aluminium a de nombreuses applications industrielles. Voici quelques-unes des plus courantes :
Céramique
L'oxyde d'aluminium est une matière première importante, couramment utilisée dans la fabrication industrielle de céramiques. Par exemple, les revêtements céramiques pour automobiles sont fabriqués à partir d'oxyde d'aluminium.
Céramiques techniques
Dans le domaine des céramiques techniques, l'alumine est principalement utilisée pour la fabrication de composants hautes performances. Ces céramiques nécessitent généralement une pureté d'alumine de 99,51 TP3T, voire supérieure, pour atteindre des performances optimales.
Par exemple, dans les équipements de fabrication de semi-conducteurs, la céramique d'alumine peut être utilisée pour fabriquer des supports de plaquettes et d'autres composants, grâce à l'excellente résistance aux températures élevées et à la corrosion de l'alumine.
Dans la fabrication d'instruments de précision, l'alumine est également utilisée pour fabriquer des sondes de mesure et des composants de capteurs, en raison de sa stabilité dimensionnelle et de sa résistance à l'usure.

Céramiques d'alumine
Céramiques structurelles
Les principales utilisations de la céramique structurelle sont la portance et la protection. En génie mécanique, les roulements et joints en oxyde d'aluminium témoignent de leur résistance à l'usure unique, et leur durée de vie supérieure les rend également efficaces dans les équipements rotatifs à grande vitesse.
Dans le domaine de la protection, l'alumine est utilisée dans les équipements militaires. Dotée d'une dureté et d'une ténacité exceptionnelles, cette armure constitue un élément essentiel des équipements de protection militaires.

Céramique pare-balles
Applications biomédicales
L'alumine peut être utilisée comme biomatériau pour remplacer les tissus endommagés du corps humain, notamment les organes tels que les membres, les mains, les os et les articulations. De même, vous pouvez appliquer vos connaissances en biomatériaux aux dispositifs électroluminescents utilisés en milieu hospitalier, par exemple pour traiter les cellules cancéreuses nécessitant de la lumière pour guérir.
Organes artificiels
L'alumine est principalement utilisée dans le domaine biomédical pour les articulations artificielles et les implants dentaires. Dotée d'une bonne biocompatibilité, elle constitue un matériau idéal pour les implants médicaux.
Lors de certaines interventions de remplacement de la hanche, les têtes sphériques en céramique d'alumine offrent un coefficient de frottement plus faible et une bonne résistance à l'usure. Ces dernières années, les matériaux composites à base d'alumine ont également réalisé des avancées significatives dans le domaine de la restauration dentaire.
Dispositifs médicaux
To comply with strict industry regulations, these devices often feature permanent medical laser marking for unique device identification (UDI). In addition to human implants, alumina is also widely used to manufacture surgical instruments and diagnostic equipment parts. These devices usually require excellent cleaning and sterilization properties, and the chemical stability and non-toxicity of alumina just meet these needs. In addition, in medical imaging equipment, alumina ceramic windows are also widely used because of their good X-ray transmittance.
Matériaux réfractaires
La fabrication de matériaux réfractaires dépend fortement de l'oxyde d'aluminium comme matière première. Cela est dû aux propriétés physiques et chimiques spécifiques de l'alumine, telles que :
- Excellente résistance à la traction et mécanique,
- Bonne conductivité thermique.
- Point d'ébullition et de fusion élevé.
- Résistance à la corrosion et aux produits chimiques.
- Utilisations de l'alumine dans les applications réfractaires
L'alumine est largement utilisée dans diverses applications réfractaires, notamment dans l'industrie du ciment, la fabrication du verre et de l'acier.
Industrie du ciment
Dans la production de ciment, les matériaux réfractaires en alumine sont principalement utilisés pour le revêtement des fours rotatifs. L'alumine résiste à des températures élevées supérieures à 1 450 °C et à une forte corrosion chimique, ce qui la rend très utile dans ces environnements difficiles. L'utilisation de briques d'alumine de haute pureté permet de prolonger considérablement la durée de vie du four et de réduire les temps d'arrêt pour maintenance.
Fabrication du verre
L'utilisation de matériaux réfractaires en alumine dans les fours de fusion du verre offre une excellente résistance à la corrosion et une bonne stabilité thermique. L'alumine de haute pureté conserve sa structure complète à 1600 °C, ce qui empêche efficacement la pénétration et l'érosion du verre liquide. Utilisés en grandes quantités, ces matériaux réfractaires peuvent prolonger considérablement la durée de vie de votre four.
Métallurgie du fer et de l'acier
Dans l'industrie sidérurgique, les matériaux réfractaires à base d'alumine peuvent être utilisés dans les systèmes de coulée et les zones de travail à haute température. Ces zones doivent généralement résister à l'érosion et aux chocs thermiques du métal en fusion. Or, les matériaux à base d'alumine de haute pureté résistent bien aux chocs thermiques, garantissant ainsi le fonctionnement sûr des équipements de fusion.

Billes et briques réfractaires à haute teneur en alumine
Électronique
L'oxyde d'aluminium est une matière première importante dans la fabrication de divers appareils électroniques. L'alumine offre généralement de bonnes propriétés isolantes, essentielles pour éviter les chocs électriques.
C'est pourquoi il est couramment utilisé dans les disjoncteurs. Parmi les autres applications où l'oxyde d'aluminium est utilisé en électronique, on peut citer résistances, et des condensateurs.
Composants du circuit
Dans l'industrie électronique, l'alumine peut être utilisée comme substrat. Ses excellentes propriétés de dissipation thermique et d'isolation peuvent devenir un matériau important pour l'encapsulation des circuits intégrés. Les propriétés supérieures des substrats en alumine peuvent notamment être exploitées pour améliorer considérablement les performances de certains dispositifs LED et radiofréquences de forte puissance.
Matériaux isolants
L'alumine possède des propriétés isolantes et peut être utilisée comme matériau isolant. Elle est largement utilisée comme isolant dans les équipements électriques haute tension.

Circuit à couche mince en alumine
Abrasifs
Dans le domaine des abrasifs, l'oxyde d'aluminium est le matériau privilégié pour divers types de meulage haut de gamme. Sa dureté et sa ténacité exceptionnelles en font un excellent matériau de meulage. Pour certains procédés de traitement de surface du métal et du bois, les abrasifs à base d'oxyde d'aluminium constituent un choix quasi idéal.
Lectures complémentaires : Abrasif à l'oxyde d'aluminium vs abrasif au carbure de silicium
Lectures complémentaires : Autres utilisations de l'alumine
Conclusion
En résumé, l’oxyde d’aluminium est l’un des oxydes métalliques les plus précieux présents naturellement à la surface de la Terre.
Il contient diverses propriétés chimiques et physiques qui le rendent adapté à de nombreuses applications industrielles.
FAQ
Vous trouverez ci-dessous les questions fréquemment posées sur l’oxyde d’aluminium en tant que composé métallique.
1. L’oxyde d’aluminium est-il toxique pour l’homme ?
D'un point de vue médical, l'oxyde d'aluminium est moins toxique pour le corps humain et peut être considéré comme non toxique car l'ingestion d'oxyde d'aluminium ne provoque pas de problèmes de santé graves.
Le contact quotidien avec l'oxyde d'aluminium est sans danger. Cependant, il est déconseillé d'ingérer de l'oxyde d'aluminium, car celui-ci peut provoquer des problèmes de santé mineurs tels que maux de tête, nausées, toux et vomissements. Par conséquent, l'oxyde d'aluminium ne doit pas être ingéré par le corps humain.
Lectures complémentaires : L'oxyde d'aluminium est-il toxique ?
2. Pourquoi l’oxyde d’aluminium est-il cher ?
Comparé à d’autres oxydes métalliques, l’oxyde d’aluminium est l’un des composés métalliques les plus chers.
La production d’oxyde d’aluminium nécessite beaucoup d’énergie, ce qui a un impact significatif sur le coût.
Cela explique pourquoi l'aluminium est très valorisé par rapport aux autres métaux. En général, son coût élevé compense le coût du procédé de production.
3. L’oxyde d’aluminium est-il sûr ?
La sécurité de l'oxyde d'aluminium reste un mystère pour beaucoup. Pourtant, il a été prouvé qu'il est sans danger pour l'homme.
Dans certaines situations rares, il existe des effets secondaires chez les personnes utilisant ce composé d'aluminium.
Par exemple, une insuffisance pulmonaire due à l’inhalation de poudre d’aluminium, ainsi qu’une irritation des yeux et de la peau.